Les bonbons
3) Identification de la molécule du sucre utilisé pour l'expérience
3. Identification de la molécule du sucre utilisé pour l’expérience
3.1. La structure moléculaire du sucre utilisé
Pour notre expérience nous avons utilisé du saccharose appelé plus généralement « sucre de table » ou « sucre blanc ». Il peut être utilisé dans son apparence brute pour sucrer des pâtisseries, ou juste son café le matin. Ce sucre de table a su s’imposer au fil des années, et est devenu incontournable pour la majorité des foyers. Mais on retrouve également le saccharose dans divers aliments comme le sirop d’érable ou les fruits.
Comme dit précédemment (cf. III.1.1.1.), le saccharose est un diholoside qui a comme formule brute : C12H22O11. C’est un sucre non réducteur qui a une masse molaire de 342,3 g/mol. Son nom chimique : β-D-fructofuranosyl-(2↔1)-α-D-glucopyranoside, nous indique qu’on a bien une association de glucose et de fructose relié par une liaison osidique (liaison chimique entre deux ose, un ose étant un sucre) : (2↔1).
Comme cette molécule de sucre a la faculté de cristalliser facilement, on l’utilise pour la fabrication du « sucre cristallisé », vendu dans le commerce. Après le fructose, c’est le glucide le plus sucré au niveau du goût, d’où son intérêt pour l’industrie alimentaire. Ce sucre caramélise à 160° et a une solubilité qui varie en fonction de la température, plus celle-ci est grande et plus il est soluble :
La dissolution est possible car les composants du saccharose sont favorables à la fusion entre les molécules d’eau et celles de saccharose. (Explication ci-dessous avec les oses qui composent le saccharose : le glucose et le fructose). Cette solubilité est avantageuse pour les gourmands qui veulent adoucir leur nourriture, principalement les boissons comme le thé ou le café. Elle est également avantageuse et pratique dans la fabrication des bonbons, car, un composé qui se dissout bien, ne nécessite pas diverses étapes pour unifier les mélanges chimiques.
3.2. La comparaison avec d’autres molécules de sucre
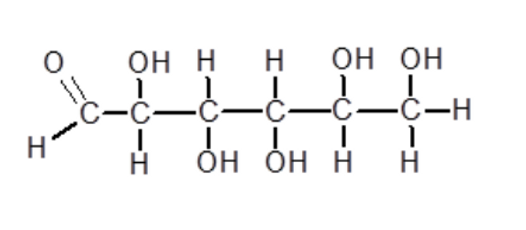
Le glucose, le fructose et le galactose sont 3 oses isomères c'est-à-dire de même formule brute: C6O6H12 (6 carbones, 6 oxygènes et 12 hydrogènes) mais de formules développées et topologiques différente. Ces 3 monoholosides ont une masse malaire de 180g.mol-1.
Exemple : formule développée du galactose
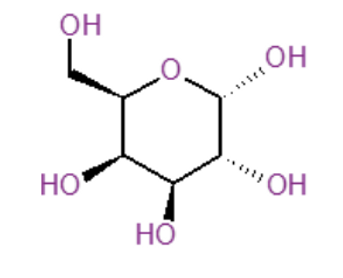
Les oses sont généralement présents sous une forme cyclique et acyclique (cycle de 5 ou 6 atomes), leur pouvoir sucrant varie entre eux, mais est toujours estimé en fonction de celui du saccharose qui sert de référence, avec un pouvoir sucrant de 100.
Représentation cyclique du glucose
Le Glucose a un pouvoir sucrant de 70-75. Sa solubilité varie en fonction de la température, comme pour le saccharose, mais est cependant très inférieure à ce dernier. Par exemple, la solubilité du glucose dans l’eau est de 70g dans 100ml d’eau à 20°.
Le fructose a un pouvoir sucrant très élevé de 130 à 150, il est également plus soluble dans l’eau que le glucose avec 375g dans 100ml d’eau à 20°C.
Le galactose a un pouvoir sucrant de 30, plus faible que celui du glucose. Il ne constitue pas une source d'énergie directement utilisable par le corps, du fait qu’il doit d'abord être transformé en glucose par le foie. Il n’est pas très soluble dans l'eau et est peu recherché pour sa qualité sucrante.
Ce sont tous les trois des glucides simples, ces derniers ont en général les propriétés suivantes :
-
La molécule sera facilement solubilisée dans l’eau en présence des groupements hydroxyles : –OH qui sont très hydrophile (qui ont de l’affinité avec l’eau).
-
Grâce à la présence de la double liaison C=O qui a une fonction «réductrice»: mise en évidence facile de la présence des monoholosides.
Formule développée du glucose
3.3. Qu’est ce qui dans la molécule du sucre est à l’origine du goût sucré
« Le saccharose fait partie des glucides simples, qui ont une structure peu complexe et sont donc plus rapidement absorbés par l’organisme. Ce sont des sucres dits « rapides ». Une structure en hexagone est présente dans chaque molécule observée et le nombre de ces structures varie en fonction du pouvoir sucrant de la molécule. Ce noyau joue-t-il un rôle prépondérant dans le goût que procurent ces sucres ? »
Le monde du vivant, William K. Purves/David Sadava/ Gordon H. Orians
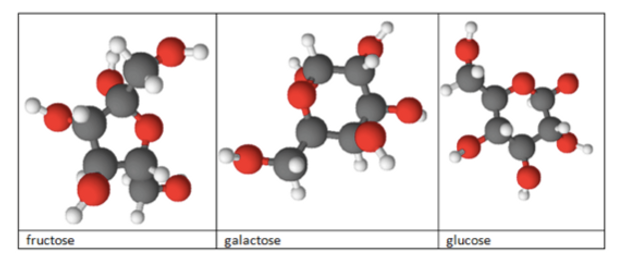
Beaucoup de scientifiques ont émis des hypothèses sur l’origine du goût sucré. Une des théories les plus pertinentes est que cette origine serait liée la structure des molécules de sucres. Prenons l’exemple des sucres vu précédemment et de la stévia qui, bien que n’étant pas un glucide, a quand même un pouvoir sucrant (cf. schémas et descriptions ci-dessous). Nous pouvons observer que toutes ces molécules ont en commun une structure de forme hexagonale en cycle. Celle-ci est bien visible et peut être présente plusieurs fois dans la même molécule. Il est également possible de faire le rapprochement entre la présence de cette structure en cycle et le pouvoir sucrant d’une molécule. En effet, plus il y a de structures hexagonales et plus le pouvoir sucrant de la molécule est élevée. La présence de ce cycle aromatique pourrait donc être la cause du goût sucré de la molécule et son nombre ferait augmenter le pouvoir sucrant de cette dernière. Bien que tout ceci reste une hypothèse émise par de nombreux scientifiques, il faut avouer qu’elle est plutôt cohérente.
Schémas des structures de différentes molécules de sucres ainsi que de la stévia
(Sont détaillés ci-dessus : les atomes de carbone en gris, les atomes d’oxygène en rouge et les atomes hydrogène en blanc.)
Représentation du cycle aromatique présent dans les molécules de sucre y compris la stévia
Nous pouvons donc poser l’hypothèse que l’origine du goût sucré serait liée à la présence d’un ou de plusieurs cycles aromatiques dans les molécules de sucre.